Laboratoryjne metody diagnostyki zakażeń Clostridioides difficile jako ważny aspekt w leczeniu i kontroli CDI

Główne czynniki ryzyka wystąpienia CDI
Poznano wiele czynników ryzyka wystąpienia CDI, a do najistotniejszych zaliczamy antybiotykoterapię. Poszczególne grupy antybiotyków charakteryzują się różnym ryzykiem wystąpienia CDI. Podział w zależności od stopnia ryzyka wystąpienia CDI znajduje się w tab. 2.
Innym ważnym czynnikiem jest długotrwałe stosowanie antagonistów receptora H2 lub inhibitorów pompy protonowej, które poprzez obniżenie kwasowości żołądka uniemożliwiają eliminację przetrwalników CD.
Ponadto są to: długa hospitalizacja, operacje – szczególnie w obrębie przewodu pokarmowego, poprzednie epizody CDI, zaawansowany wiek, chemioterapia, HIV, choroby zapalne jelit, hipoalbuminemia, choroby nerek, przeszczepy narządów oraz niedobór witaminy D (6, 7, 8).

Materiał do badania w kierunku zakażenia C. difficile
Materiałem do badania powinny być jedynie płynne lub nieuformowane stolce, czyli próbki kału przyjmujące kształt pojemnika. Do badania nie należy pobierać próbek kału uzyskanych po podaniu środków przeczyszczających. Wybór odpowiedniej próbki kału do badania ma zasadnicze znaczenie, ponieważ obecnie dostępne testy nie pozwalają odróżnić CDI od bezobjawowego nosicielstwa toksynotwórczego szczepu C. difficile.
Wyjątek stanowią pacjenci z niedrożnością jelit, u których nie występuje biegunka. Pobrany wówczas wymaz z odbytu może być badany tylko technikami biologii molekularnej lub metodą posiewu.
W celu uzyskania optymalnych wyników, próbki kału powinny zostać posiane w ciągu 2 godzin od pobrania i przechowywane w szczelnym pojemniku. Po upływie tego czasu, podczas przechowywania próbki w lodówce, liczba komórek wegetatywnych istotnie się zmniejsza. W przypadku oznaczania toksyn, kał może być przechowywany w temperaturze 4°C przez maksymalnie 3 dni, później należy go zamrozić w temperaturze -80°C.
Próbki kału powinny być pobrane przed rozpoczęciem leczenia, aby uniknąć wyników fałszywie ujemnych (5, 9).
Schematy diagnostyczne zakażeń Clostridioides difficile
Obecnie nie istnieje jeden pojedynczy szybki test zatwierdzony przez FDA, który można by niezawodnie wykorzystać do diagnozowania CDI.
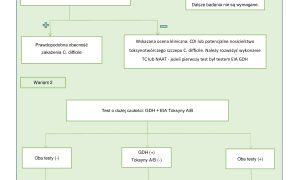
W celu wykrycia CD zarówno w USA, jak i w Europie zalecany jest dwu lub trzystopniowy algorytm postępowania (ryc. 1). W pierwszej kolejności wykonuje się test o wysokiej ujemnej wartości predykcyjnej (negative predictive value, NPV), czyli taki, który jest niezawodny wobec próbek z ujemnym wynikiem. Warunek ten spełniają testy GDH (dehydrogenazy glutaminowej – z ang. glutamate dehydrogenas) EIA i testy molekularne NAAT (metody amplifikacji kwasów nukleinowych – z ang. nucleic acid amplification tests). Ujemny wynik testu oznacza małe prawdopodobieństwo CDI, a dalsze badania nie są wymagane. Wynik pozytywny wymaga dalszej diagnostyki i wykonania kolejnych badań w celu wykrycia obecności toksyn C. difficile. Testy te z kolei powinny charakteryzować się wysoką dodatnia wartością predykcyjną (positive predictive value, PPV), czyli być prawdziwie dodatnimi, np. test toxin A/B EIA, NAAT, TC (toxigenic culture).
Dopuszcza się także zastosowanie testu kombinowanego, który wykrywa jednocześnie GDH i toksyny CD. Diagnostykę należy oprzeć przede wszystkim na stwierdzeniu objawów klinicznych i analizie wyników badań diagnostycznych. Pamiętając o tym, że leczymy pacjenta, a nie wynik, decyzja o wprowadzeniu leczenia powinna być podejmowana w oparciu o obraz kliniczny chorego.
Wieloetapowe algorytmy łączące dwa lub trzy testy zwiększają dokładność diagnostyczną zakażenia C. difficile i są zalecane. Niezbędny jest odpowiedni dobór pacjentów do badań w kierunku CDI, aby zapobiec negatywnym skutkom wykrycia przypadków kolonizacji wzrostu wskaźnika zakażeń CD w szpitalu oraz nadmiernej kolonizacji i zakażeń drobnoustrojami wielolekoopornymi u pacjentów, którzy niepotrzebnie otrzymali leczenie antybiotykami nieistniejącego zakażenia CD (5, 10, 11).
Laboratoryjne metody wykrywania CD
Hodowla szczepu toksynotwórczego – TC
TC jest to metoda oparta na wyhodowaniu szczepu C. difficile z próbek kału i stwierdzeniu, czy wyizolowany szczep jest izolatem wytwarzającym toksyny. W tym celu stosuje się różnorodne podłoża mikrobiologiczne (np.: agar CCFA, agar Braziera, CHROMID C. difficile agar), które inkubujemy od 48h do 7 dni w warunkach beztlenowych. Aby zwiększyć szanse na wyhodowanie szukanego szczepu i kiełkowanie spor, badany materiał poddaje się szokowi alkoholowemu lub cieplnemu. Wyhodowane kolonie C. difficile przyjmują barwę od żółtawej do białej o postrzępionych brzegach, sprawiające wrażenie szklistych, wykazują charakterystyczny koński zapach oraz żółto-zieloną fluorescencję w świetle lampy Wooda. Ostateczną identyfikację opiera się na wykonaniu testów biochemicznych lub z udziałem innych metod, na przykład chromatograficznych, MALDI – TOF. Wyhodowane szczepy C. difficile należy poddać dalszym badaniom w celu wykazania ich toksynotwórczości. W tym celu należy stosować metodę referencyjną – test neutralizacji cytotoksyczności (CCNA). Połączenie techniki hodowlanej wraz z testem CCNA stanowi metodę referencyjną w diagnostyce CDI, stanowi ona też metodę odniesienia w stosunku do innych dostępnych testów, jednak z powodu m.in. długiego czasu oczekiwania na wynik (2 – 5 dni) nie jest stosowana w rutynowej diagnostyce. Hodowla szczepu C. difficile posiada pewne zalety, ponieważ umożliwia typowanie badanego szczepu i oznaczenie jego lekowrażliwości (11, 12).
Czytaj też: Rozwój diagnostyki laboratoryjnej szansą na zwiększenie efektywności systemu opieki zdrowotnej