Technologia jako „co-pilot” kliniczny. Rola sztucznej inteligencji w anestezjologii i intensywnej terapii – wyzwania, szanse, granice

Sztuczna inteligencja nie zastępuje anestezjologa. Zmienia jednak sposób, w jaki widzi on pacjenta, i odpowiedzialność, jaką za tę wizję ponosi.
Jeszcze kilkanaście lat temu ultrasonografia w anestezjologii i intensywnej terapii była postrzegana głównie jako narzędzie pomocnicze – wykorzystywane bardzo często doraźnie i zależne niemal wyłącznie od indywidualnych kompetencji operatora. Dziś sytuacja ta uległa zasadniczej zmianie. Point-of-care ultrasound (POCUS) stała się jednym z kluczowych filarów nowoczesnej anestezjologii i intensywnej terapii, oraz medycyny ratunkowej, a jej znaczenie rośnie równolegle z rozwojem technologii cyfrowych oraz systemów sztucznej inteligencji (1).
Ultrasonografia przyłóżkowa (POCUS) doskonale odpowiada na podstawowe potrzeby środowisk o wysokiej dynamice decyzyjnej: umożliwia szybkie uzyskanie informacji diagnostycznej, jest nieinwazyjna, dostępna bezpośrednio przy łóżku pacjenta i pozwala na ocenę stanu chorego w czasie rzeczywistym. W przeciwieństwie do klasycznych badań obrazowych, takich jak tomografia komputerowa czy rezonans magnetyczny, POCUS nie wymaga transportu pacjenta ani angażowania dodatkowych zasobów organizacyjnych, co w warunkach oddziału intensywnej terapii, bloku operacyjnego czy szpitalnego oddziału ratunkowego ma kluczowe znaczenie dla bezpieczeństwa i ciągłości opieki.
Jednocześnie należy podkreślić, że środowisko anestezjologii i intensywnej terapii generuje szczególnie duże obciążenie poznawcze dla personelu medycznego. Decyzje podejmowane są pod presją czasu, często na podstawie niepełnych lub dynamicznie zmieniających się danych, a klasyczne systemy monitorowania dostarczają ogromnej liczby parametrów, które wymagają szczegółowej interpretacji. W takich warunkach ryzyko błędów, opóźnień decyzyjnych czy nadmiernego polegania na intuicji klinicznej istotnie wzrasta, co wielokrotnie podkreślano w literaturze dotyczącej bezpieczeństwa pacjentów w anestezjologii i intensywnej terapii (2).
To właśnie w tym miejscu ultrasonografia, wsparta algorytmami sztucznej inteligencji, zaczyna pełnić rolę nie tylko narzędzia diagnostycznego, lecz także elementu systemu wsparcia decyzji klinicznych. Nowoczesne rozwiązania oparte na uczeniu maszynowym i głębokich sieciach neuronowych umożliwiają automatyczną identyfikację struktur anatomicznych, optymalizację ustawień aparatu, wykonywanie złożonych pomiarów oraz analizę trendów hemodynamicznych w czasie rzeczywistym. W efekcie ultrasonografia przestaje być jedynie „obrazem”, a staje się źródłem przetworzonej informacji klinicznej, gotowej do wykorzystania w procesie decyzyjnym.
W literaturze coraz częściej podkreśla się, że POCUS jest technologią szczególnie predysponowaną do integracji ze sztuczną inteligencją. Wynika to z kilku kluczowych cech: standaryzacji projekcji, powtarzalności protokołów badania, możliwości pracy na obrazach w skali szarości oraz ogromnej dostępności danych obrazowych, które mogą być wykorzystywane do trenowania algorytmów. W przeciwieństwie do wielu innych metod diagnostycznych, ultrasonografia pozwala na szybkie generowanie dużej liczby danych w warunkach rzeczywistej praktyki klinicznej, co znacząco przyspiesza rozwój i walidację systemów AI (3).
Z perspektywy organizacyjnej i systemowej ultrasonografia wspierana przez sztuczną inteligencję odpowiada również na jedno z największych wyzwań współczesnej medycyny – nierównomierny poziom kompetencji personelu oraz ograniczoną dostępność ekspertów. Badania pokazują, że rozwiązania AI-wspierające POCUS mogą istotnie zmniejszać różnice pomiędzy operatorami o różnym poziomie doświadczenia, poprawiając powtarzalność wyników i bezpieczeństwo procedur, szczególnie w środowiskach o ograniczonych zasobach kadrowych (4).
Z mojego doświadczenia dydaktycznego i obserwacji klinicznych wynika, że właśnie w ultrasonografii najbardziej widoczna jest zmiana paradygmatu: od technologii wymagającej wieloletniej nauki pod okiem eksperta do narzędzia, które, przy odpowiednim wsparciu algorytmów, może być efektywnie wykorzystywane przez szerokie grono lekarzy. Nie oznacza to oczywiście uproszczenia odpowiedzialności klinicznej, lecz raczej jej przesunięcie: z manualnej obsługi aparatu w stronę krytycznej oceny informacji dostarczanej przez system.
Dlatego ultrasonografia stała się dziś naturalnym punktem wyjścia dla wdrażania sztucznej inteligencji w anestezjologii i intensywnej terapii. Jest technologią „bliską pacjentowi”, osadzoną w codziennym workflow, a jednocześnie wystarczająco dojrzałą technologicznie, by pełnić rolę klinicznego „co-pilota” – systemu, który nie zastępuje lekarza, lecz wspiera go w podejmowaniu coraz bardziej złożonych decyzji w coraz bardziej wymagającym środowisku.
POCUS wspierane przez sztuczną inteligencję – od obrazu do interpretacji
Point-of-care ultrasound przez wiele lat pozostawało narzędziem silnie zależnym od doświadczenia operatora. Jakość obrazu, poprawność identyfikacji struktur anatomicznych oraz wartość kliniczna badania były w dużej mierze funkcją indywidualnych kompetencji lekarza, jego znajomości sonoanatomii oraz umiejętności pracy pod presją czasu. W praktyce prowadziło to do istotnej zmienności międzyoperatorskiej oraz ograniczało możliwość systemowego wykorzystania POCUS w anestezjologii i intensywnej terapii oraz medycynie ratunkowej (1).
Rozwój sztucznej inteligencji w ultrasonografii zmienia ten paradygmat. Współczesne rozwiązania AI nie ograniczają się już wyłącznie do poprawy jakości obrazu czy automatycznej regulacji parametrów aparatu. Ich zasadniczą rolą staje się przekształcenie obrazu ultrasonograficznego w ustrukturyzowaną informację kliniczną, możliwą do bezpośredniego wykorzystania w procesie decyzyjnym. Tym samym ultrasonografia przestaje być jedynie narzędziem obrazowania, a zaczyna pełnić funkcję elementu systemu wsparcia decyzji klinicznych (3, 5). W tym ujęciu ultrasonografia wsparta AI przestaje być wyłącznie narzędziem diagnostycznym, a zaczyna pełnić funkcję elementu ciągłego monitorowania stanu pacjenta.
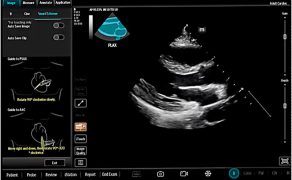
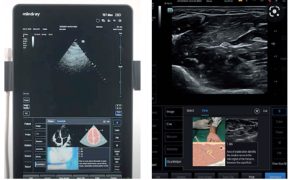
Proces ten rozpoczyna się już na etapie akwizycji obrazu. Algorytmy sztucznej inteligencji coraz częściej pełnią funkcję systemów prowadzenia użytkownika, pomagając w prawidłowym ustawieniu głowicy, doborze optymalnej projekcji oraz stabilizacji obrazu. Ma to szczególne znaczenie w warunkach intensywnej terapii i bloku operacyjnego czy szpitalnego oddziału ratunkowego, gdzie badania POCUS wykonywane są często w pośpiechu, w nieidealnych warunkach sonoanatomicznych i organizacyjnych. Dzięki temu możliwe staje się uzyskanie diagnostycznie użytecznych obrazów również przez lekarzy z mniejszym doświadczeniem ultrasonograficznym, bez obniżenia jakości badania (6).
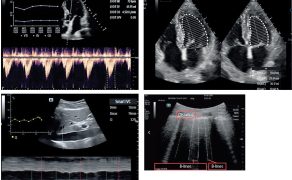
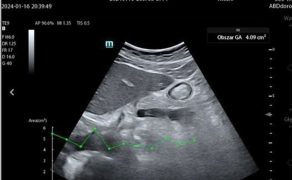
Kolejnym krokiem jest automatyczna identyfikacja struktur anatomicznych oraz wykonywanie złożonych pomiarów, które dotychczas wymagały wysokiej biegłości technicznej. W praktyce klinicznej obejmuje to m.in. automatyczną ocenę funkcji skurczowej serca, analizę przepływów, ocenę zmienności wymiarów naczyń czy identyfikację charakterystycznych artefaktów płucnych. Z punktu widzenia anestezjologii i intensywnej terapii kluczowe znaczenie ma fakt, że pomiary te wykonywane są szybko, powtarzalnie i w sposób ustandaryzowany, co znacząco ogranicza zmienność między operatorami i poprawia bezpieczeństwo podejmowanych decyzji (4).
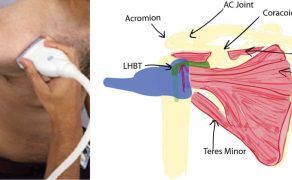
Jednym z najbardziej przełomowych elementów tej transformacji jest rozwój systemów automatycznego labelingu, czyli kolorowego kodowania struktur anatomicznych w czasie rzeczywistym. Rozwiązania te, oparte na algorytmach uczenia maszynowego i głębokich sieciach neuronowych (m.in. architekturze U-Net), umożliwiają automatyczne rozpoznawanie i oznaczanie kluczowych struktur, takich jak nerwy, naczynia, mięśnie, powięzi czy opłucna, przy użyciu czytelnego kodu kolorystycznego. W efekcie obraz ultrasonograficzny przestaje być jedynie płaską reprezentacją anatomii, a zaczyna pełnić funkcję interaktywnego interfejsu informacyjnego (6).
Z perspektywy anestezjologii szczególne znaczenie ma zastosowanie labelingu w regionalnych technikach znieczulenia oraz w procedurach wykonywanych pod kontrolą ultrasonografii. Kolorowe oznaczenie struktur pełni wówczas funkcję swoistego head-up display, który w czasie rzeczywistym wspiera orientację przestrzenną operatora i zmniejsza ryzyko przypadkowego uszkodzenia struktur krytycznych. Badania wskazują, że tego typu rozwiązania mogą skracać czas wykonywania procedur, zwiększać ich bezpieczeństwo oraz zmniejszać zależność jakości zabiegu od doświadczenia operatora (2, 6).
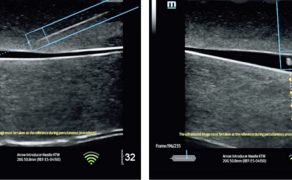
Naturalnym uzupełnieniem systemów labelingu są technologie umożliwiające precyzyjną identyfikację i śledzenie położenia igły w czasie rzeczywistym. W klasycznej ultrasonografii prowadzenie igły pod kontrolą obrazu wymaga jednoczesnej kontroli osi wiązki ultradźwiękowej, kąta wkłucia oraz relacji igły do struktur krytycznych, co stanowi istotne obciążenie poznawcze nawet dla doświadczonych operatorów. Nowoczesne systemy nawigacji igły wykorzystują magnetyczną identyfikację jej położenia względem płaszczyzny obrazowania, dostarczając jednoznacznej informacji zwrotnej dotyczącej trajektorii wkłucia i położenia końcówki igły (1).
Z klinicznego punktu widzenia rozwiązania te pełnią rolę aktywnego wsparcia orientacji przestrzennej, szczególnie w regionalnych technikach znieczulenia, kaniulacjach naczyń zarówno centralnych, jak i obwodowych oraz procedurach wykonywanych w bezpośrednim sąsiedztwie struktur krytycznych. Połączenie magnetycznej identyfikacji igły z labelingiem struktur anatomicznych tworzy spójny ekosystem interpretacyjny, w którym lekarz otrzymuje odpowiedź zarówno na pytanie „co widzę?”, jak i „gdzie znajduje się igła i dokąd zmierza?” (1, 6).
Najistotniejsza zmiana zachodzi jednak na poziomie interpretacji danych. Tradycyjnie ultrasonografia była narzędziem opisowym, a lekarz samodzielnie formułował hipotezy diagnostyczne na podstawie obserwowanego obrazu. Współczesne systemy AI przesuwają ten proces w kierunku interpretacji wspomaganej algorytmicznie, w której obraz ultrasonograficzny integrowany jest z innymi danymi klinicznymi i prezentowany w postaci sugestii diagnostycznych, trendów lub wskaźników istotnych klinicznie. Sztuczna inteligencja porządkuje dane i zmniejsza obciążenie poznawcze lekarza, nie przejmując jednak odpowiedzialności za decyzję (2, 3, 7).
Należy jednocześnie podkreślić ograniczenia tych technologii. Zarówno labeling struktur, jak i systemy śledzenia igły oraz algorytmicznej interpretacji obrazu działają w ramach określonych zbiorów danych treningowych i mogą nieprawidłowo funkcjonować w sytuacjach nietypowych anatomicznie lub rzadkich klinicznie. Z tego powodu rozwiązania te nie mogą być traktowane jako „prawda obiektywna”, lecz jako wsparcie interpretacyjne, wymagające każdorazowej weryfikacji przez lekarza (2, 3).
Z perspektywy autora największą wartością AI-wspieranego POCUS nie jest sama automatyzacja ultrasonografii, lecz zmiana sposobu interakcji lekarza z obrazem i informacją kliniczną. Obraz przestaje wymagać żmudnego dekodowania, a zaczyna aktywnie wspierać rozumienie sytuacji klinicznej. W tym sensie ultrasonografia wsparta sztuczną inteligencją staje się jednym z najbardziej czytelnych przykładów technologii pełniącej rolę „co-pilota” klinicznego – narzędzia, które zwiększa bezpieczeństwo i przewidywalność procedur, nie odbierając lekarzowi odpowiedzialności za ostateczną decyzję.
Moja wizja: anestezjolog i intensywista w erze „inteligentnego POCUS”
Rozwój ultrasonografii point-of-care wspieranej przez sztuczną inteligencję nie oznacza zmiany jednego narzędzia na inne. Oznacza zmianę sposobu postrzegania pacjenta oraz roli lekarza w coraz bardziej złożonym środowisku klinicznym. W mojej ocenie „inteligentny POCUS” stanie się w najbliższych latach standardem pracy anestezjologa i intensywisty, podobnie jak standardem stały się dziś ciągłe monitorowanie parametrów życiowych czy nowoczesna wentylacja mechaniczna.
Anestezjolog przyszłości nie będzie definiowany wyłącznie przez biegłość manualną czy zdolność szybkiego reagowania w sytuacjach krytycznych. Kluczową kompetencją stanie się umiejętność interpretowania zintegrowanych informacji: obrazu ultrasonograficznego, danych liczbowych, trendów oraz algorytmicznych podpowiedzi. Inteligentny POCUS nie zastąpi doświadczenia klinicznego, ale sprawi, że decyzje będą podejmowane w oparciu o pełniejszy i bardziej uporządkowany obraz stanu pacjenta.
Widzę w tym także istotny wymiar systemowy. Technologie wspierane przez AI mają potencjał do wyrównywania jakości opieki, niezależnie od miejsca, pory dnia czy poziomu doświadczenia pojedynczego operatora. Dobrze zaprojektowany system nie eliminuje różnic kompetencyjnych, ale ogranicza ich negatywne konsekwencje dla bezpieczeństwa pacjenta. W tym sensie inteligentny POCUS może stać się jednym z filarów standaryzacji jakości w anestezjologii i intensywnej terapii.
Jednocześnie rozwój tych technologii przesuwa granicę odpowiedzialności. Lekarz, korzystając z narzędzi opartych na sztucznej inteligencji, nie oddaje decyzji algorytmowi, lecz bierze odpowiedzialność także za świadome korzystanie z jego wskazań. Umiejętność krytycznej oceny sugestii systemu, rozumienie jego ograniczeń oraz właściwe zarządzanie zaufaniem do technologii staną się równie istotne jak znajomość anatomii czy fizjologii.
W mojej wizji anestezjolog i intensywista ery inteligentnego POCUS to specjalista, który nie rywalizuje z technologią, lecz potrafi ją wykorzystać jako narzędzie zwiększające bezpieczeństwo, precyzję i przewidywalność swoich działań. Technologia nie zmniejsza tu roli lekarza – przeciwnie, czyni ją bardziej odpowiedzialną.
Podsumowanie
Sztuczna inteligencja nie zastępuje anestezjologa. Zmienia jednak sposób, w jaki widzi on pacjenta, i odpowiedzialność, jaką za tę wizję ponosi. W świecie narastającej złożoności danych, presji czasu i rosnących oczekiwań wobec jakości opieki, inteligentne technologie nie są już dodatkiem, lecz koniecznością. Kluczowe pytanie nie brzmi dziś, czy sztuczna inteligencja znajdzie miejsce w anestezjologii i intensywnej terapii, lecz jak mądrze i odpowiedzialnie ją tam wprowadzimy. Odpowiedź na to pytanie zdecyduje nie tylko o przyszłości technologii, ale przede wszystkim o bezpieczeństwie i jakości opieki nad pacjentem.
Sławomir Mika
prezes zarządu Medica Sp. z o.o., Górnośląska Szkoła Ultrasonografii w Chorzowie, członek Polskiego Towarzystwa Anestezji Regionalnej i Leczenia Bólu
Czytaj także: Nowoczesne technologie medyczne wykorzystywane w Oddziałach Anestezjologii i Intensywnej Terapii
Galeria
Komentarze
Mogą zainteresować Cię również
Strefa wiedzy
721 praktycznych artykułów - 324 ekspertów - 16 kategorii tematycznych