Rola akredytowanego laboratorium w procesie potwierdzania bezpieczeństwa wyrobów medycznych

O zdolności laboratorium do badania wyrobów medycznych według norm zharmonizowanych z Dyrektywą Rady 93/42/EWG dotyczącą wyrobów medycznych decyduje Polskie Centrum Akredytacji, nadając przedmiotową akredytację (dla TÜV Rheinland Polska akredytacja nr AB 904).
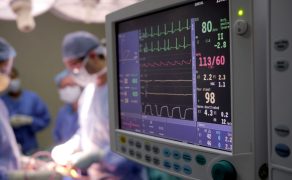
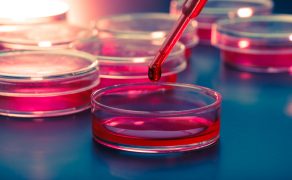
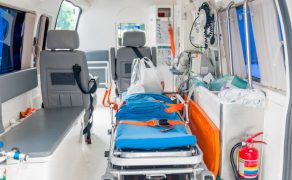
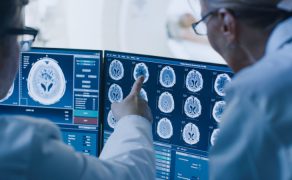
Rynek wyrobów medycznych to obszar nadzorowany w każdym kraju świata, również w Polsce. Wytwórców wyrobów medycznych oraz produkowane i wprowadzane do obrotu wyroby medyczne kontroluje się głównie z uwagi na ochronę rodzimego rynku przed konkurencją z zewnątrz, potwierdzenie skuteczności wyrobu medycznego w zakresie deklarowanym przez producenta (wyrób musi mieć potwierdzoną skuteczność kliniczną na podstawie danych klinicznych) oraz w celu potwierdzenia bezpieczeństwa wyrobu medycznego (wyrób nie może zagrażać życiu i zdrowiu pacjenta, użytkownika, lekarza, pielęgniarki, ale także serwisanta czy osoby transportującej i instalującej). Na całym świecie najważniejszą rolę w procesie potwierdzania bezpieczeństwa wyrobów medycznych odgrywają laboratoria akredytowane.
O zdolności laboratorium do badania wyrobów medycznych według norm zharmonizowanych z Dyrektywą Rady 93/42/EWG dotyczącą wyrobów medycznych decyduje Polskie Centrum Akredytacji, nadając przedmiotową akredytację (dla TÜV Rheinland Polska akredytacja nr AB 904). Dzięki niej raport z badań zawierający pozytywny rezultat jest uznawany przez wszystkie inne jednostki notyfikowane. To jeden z podstawowych wymogów, aby wyrób medyczny mógł zostać wprowadzony do obrotu na rynku Unii Europejskiej.
Ważne normy w [...]
Komentarze
Strefa wiedzy
712 praktycznych artykułów - 324 ekspertów - 16 kategorii tematycznych